Nuklearmedizin: Durchführung und Nebenwirkungen der Radionuklidtherapie
Wie läuft die Behandlung ab? Welche Risiken gibt es?
In der Nuklearmedizin werden Tumoren mit radioaktiven Medikamenten behandelt. Ärzte sprechen von einer Radionuklidtherapie. Man erhält als Patient einen radioaktiven Stoff, der sich im Tumor anreichert: Radioaktive Strahlung zerstört so die Tumorzellen von innen heraus.
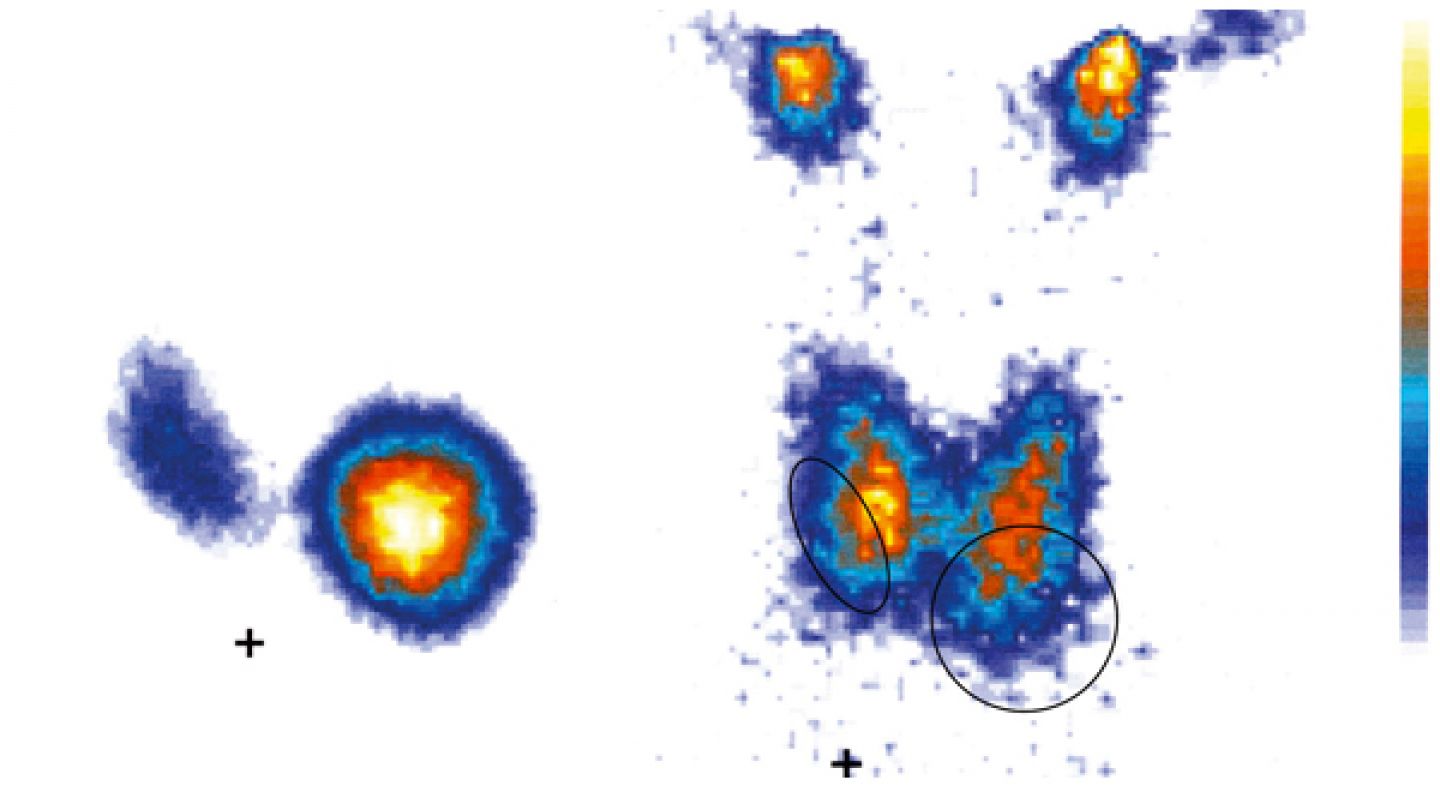
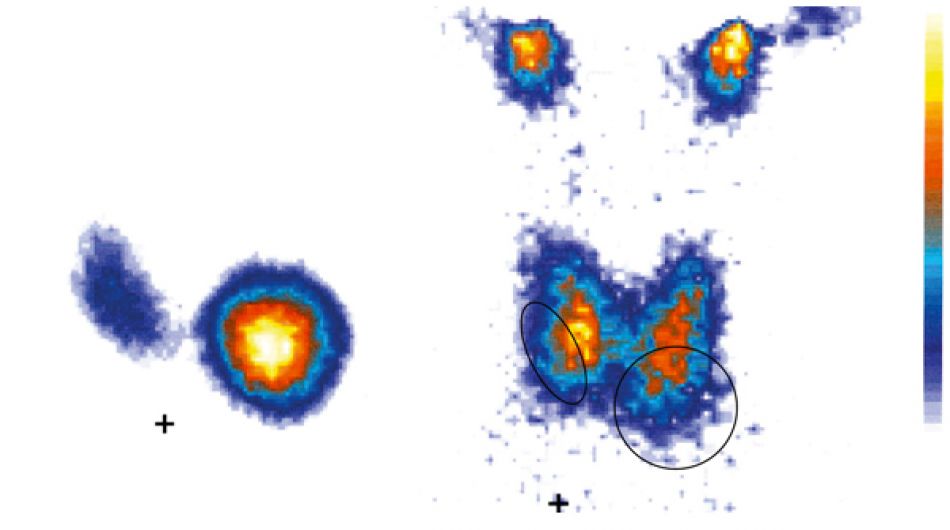
Neben der Behandlung sind Fachärzte für Nuklearmedizin auch für Untersuchungsverfahren zuständig, bei denen radioaktive Stoffe verwendet werden. Beispiele sind die Szintigraphie und die Positronen-Emissions-Tomographie. Mithilfe dieser Methoden können zum Beispiel Krebsherde im Körper aufgespürt und sichtbar gemacht werden.
Der folgende Text gibt einen Überblick über Anwendungsmöglichkeiten, Ablauf und Nebenwirkungen der Radionuklidtherapie. Er richtet sich an Patienten, Angehörige und Interessierte.
Nuklearmedizin: Was passiert bei der Radionuklidtherapie?
Bei der Radionuklidtherapie wird ein strahlendes Medikament in den Körper eingebracht, ein sogenanntes Radiopharmakon. Über das Blut gelangt es direkt zu den Tumorzellen. Die strahlende Substanz wird entweder von den Krebszellen aufgenommen oder dockt an diesen an. Dort zerfällt sie und dabei wird Strahlung frei.
Wie funktioniert das genau? Als Radiopharmaka werden Substanzen eingesetzt, die sich nicht beliebig im ganzen Körper verteilen, sondern beispielsweise im Stoffwechsel bestimmter Gewebe eine Rolle spielen, also gezielt von den entsprechenden Zellen aufgenommen werden. So gelangt radioaktives Jod zum Beispiel vor allem in die Schilddrüse und kann zur Behandlung von Schilddrüsenkrebs eingesetzt werden. Eine andere Möglichkeit: Man koppelt die strahlenden Teilchen an einen tumorspezifischen Antikörper. Dieser bindet an die Zelloberfläche der Krebszellen und bestrahlt diese von außen.
Auf diese Weise kann der Tumor mit einer hohen Strahlendosis bestrahlt werden, ohne dass gesundes Gewebe stärker geschädigt wird.
Indikation: Wann kommt eine Radionuklidtherapie infrage und wann nicht?
Am häufigsten angewendet wird die Radionuklidtherapie bei
- Schilddrüsenkrebs
- Knochenmetastasen, zur Schmerzlinderung und Vorbeugung von Knochenbrüchen.
Nuklearmedizinische Behandlungen können, wenn auch deutlich seltener, auch bei anderen Tumorarten zum Einsatz kommen, vor allem bei fortgeschrittener Erkrankung.
Wann eine Radionuklidtherapie infrage kommt und wann nicht, sollte man mit den behandelnden Ärzten besprechen.
Nicht angewendet werden darf eine Radionuklidtherapie während einer Schwangerschaft. Auch während der Stillzeit ist Vorsicht geboten: Viele der strahlenden Substanzen gehen in die Muttermilch über.
Ist eine Radionuklidtherapie bei einem eingeschränkten Gesundheitszustand möglich? Hier wägen Ärzte vor allem ab, ob das Radionuklid sich nicht nur im Tumor, sondern auch in bereits vorgeschädigten Organen anreichern könnte.
Ambulant oder stationär: Wann ins Krankenhaus?

Ob eine Radionuklidtherapie ambulant gemacht werden kann oder ob man sich dafür im Krankenhaus aufnehmen lassen muss, hängt unter anderem von dem gewählten Medikament ab. Die Behandlung von Patienten mit Knochenmetastasen ist heute weitgehend ambulant möglich. Betroffene mit einem Schilddrüsentumor müssen dagegen in die Klinik.
Wichtig dabei ist der Strahlenschutz: Für die Behandlung mit stark radioaktiven Substanzen gibt es in den Kliniken eigene Stationen. Da die strahlenden Substanzen ja auch wieder aus dem Körper ausgeschieden werden, mit dem Urin und unter Umständen auch mit dem Stuhl, muss das Abwasser gesondert gesammelt werden. Luftfilter und Unterdruck in den Räumen verhindern ein Austreten radioaktiver Strahlung.
Auf nuklearmedizinischen Stationen gelten besondere Hygienevorschriften. Das kann auch bedeuten, dass man nicht alles mit in die Klinik und vor allem nicht alles sofort wieder mit nach Hause nehmen darf. Manchmal müssen Gegenstände bis zum Abklingen der Strahlung in der Klinik aufbewahrt oder sogar entsorgt werden. Welche persönlichen Gegenstände erlaubt sind, sollte man im Vorgespräch klären.
Vor der Behandlung: Vorgespräch und Voruntersuchungen
Üblicherweise vereinbart man mit den behandelnden Ärzten einen Termin für das Vorgespräch und die notwendigen Voruntersuchungen.
- Die Ärzte benötigen alle bisherigen Befunde. Ultraschallbilder oder radiologische Bilder, wie ein Computertomogramm oder Magnetresonanztomogramm oder eine Szintigraphie, geben Auskunft über die genaue Tumorgröße und -lokalisation oder die Verteilung von Metastasen im Körper.
- Wichtig sind auch allgemeine Angaben zum Gesundheitszustand und Daten wie Körpergröße und Gewicht, um die Dosis des Medikaments zu berechnen.
- Außerdem wird meist eine Blutuntersuchung gemacht, um zum Beispiel die Nieren- und Leberfunktion oder die Schilddrüsenfunktion zu überprüfen.
Probemedikation: Patienten und Patientinnen mit Schilddrüsenkrebs erhalten vor der eigentlichen Behandlung eventuell bereits eine Probemedikation: Man schluckt eine Kapsel mit einer sehr geringen Menge an radioaktivem Jod. Die Ärzte messen, wie viel Jod von der Schilddrüse gespeichert wird. Dieser Radiojodtest kann notwendig sein, um die für die eigentliche Radiojod-Therapie individuell notwendige Jodmenge zu bestimmen.
Tumortherapie: Wie wirkt die eigentliche Behandlung?
Je nach Wirkstoff und Lage des Tumors erhält man das Radiopharmakon entweder als Kapsel, die man schlucken muss, oder aber man bekommt das Medikament in eine Vene gespritzt. Das Medikament wird vom Körper aufgenommen und gelangt über das Blut zum Zielorgan. In bestimmten Situationen kann das Medikament auch in eine Körperhöhle oder in ein Gelenk gespritzt werden. Am Bestimmungsort angekommen, zerfällt die radioaktive Substanz und setzt Strahlung frei. Wie können die Nuklearmediziner sicherstellen, dass die Substanz vor allem den Tumor bestrahlt und nicht den ganzen Körper? Hier spielen zwei Wirkmechanismen eine Rolle:
Aufnahme in die Tumorzellen: Das Radiopharmakon gelangt über Stoffwechselprozesse in die Tumorzellen. Nicht alle Stoffe werden von allen Geweben im Körper gleichmäßig aufgenommen. Jod sammelt sich zum Beispiel besonders stark in der Schilddrüse an. Andere Stoffe lagern sich vor allem in Knochen und damit auch Knochenmetastasen ein. Viele Tumoren haben zudem einen schnelleren Stoffwechsel als gesunde Zellen. Daher reichern die strahlenden Medikamente sich vermehrt in Tumorzellen an. Dies ist beispielsweise bei der Radiojodtherapie mit Jod-131 zur Behandlung von Schilddrüsenkrebs der Fall oder bei einer Radionuklidtherapie von Knochenmetastasen. Das bedeutet im Umkehrschluss auch: Diese Form der Krebstherapie ist nur möglich bei Tumoren, die aus Geweben mit solchen Stoffwechselbesonderheiten hervorgegangen sind.
Andocken an die Tumorzellen: Nicht alle Radiopharmaka werden in die Zellen aufgenommen: andere binden an bestimmte Strukturen an der Oberfläche von Tumorzellen, zum Beispiel an Rezeptoren, die mehr von Tumorzellen als von gesunden Zellen gebildet werden. Dies ist zum Beispiel bei der Radioimmuntherapie so oder bei der Peptid-Radiorezeptor-Therapie (PRRT). Bei der Radioimmuntherapie verwendet man radioaktiv markierte Antikörper, bei der PRRT radioaktiv markierte Eiweiße. Für beide Anwendungsarten gilt: Man kann nur solche Tumoren behandeln, die besondere Merkmale aufweisen. Nur dann lassen sich gezielt Antikörper oder andere "passende" Eiweiße gegen diese Merkmale herstellen und mit Radionukliden beladen.
Sowohl die Radioimmuntherapie wie auch die Peptid-Radiorezeptor-Therapie kommen daher nur für vergleichsweise wenige Patientinnen und Patienten infrage, zum Beispiel für solche mit neuroendokrinen Tumoren oder weit fortgeschrittenem Prostatakrebs, aber auch dann nur in bestimmten Krankheitssituationen.
Verteilung über das Blut: Noch etwas anders funktioniert die selektive interne Radionuklidtherapie (SIRT) zur Behandlung von Leberkrebs und Lebermetastasen: Hier wird ein Radionuklid gezielt in die Leberarterie gespritzt. Es gelangt über die Blutgefäße in die meist gut durchbluteten Tumoren, reichert sich dort an und zerstört die Tumorzellen sowie die Gefäße, die den Tumor oder die Metastasen versorgen. Nähere Informationen zu dieser Methode sind im Text Lebermetastasen beschrieben.
Strahlenschutz in der Nuklearmedizin

Die für die Therapie wichtige Strahlung, die von der radioaktiven Substanz ausgeht, reicht nur wenige Millimeter weit. Das heißt, die Tumorzellen werden zwar durch die Strahlung zerstört, gesundes Gewebe wird jedoch weitgehend geschont.
- Beim Zerfall der radioaktiven Substanz wird jedoch auch Strahlung frei, die über den eigenen Körper hinaus geht. Das kann andere Menschen gefährden, mit denen Patientinnen und Patienten engen Kontakt haben.
- Außerdem scheiden Patienten die radioaktive Substanz für einige Zeit mit dem Stuhl, Urin, Schweiß oder der Atemluft aus. Das kann zu einer erhöhten Umweltbelastung führen.
Wie lange hält diese Gefährdung an?
Die meisten in der Nuklearmedizin genutzten radioaktiven Substanzen zerfallen innerhalb weniger Stunden oder Tage. Nach der Behandlung kontrollieren die Ärzte regelmäßig, wie viel Strahlung man noch nach außen abgibt. Erst wenn ein bestimmter Grenzwert unterschritten ist, darf man die Klinik oder Fachpraxis wieder verlassen.
Was muss man nach der Entlassung beachten?
Auch nach der Entlassung gibt man eventuell noch ein wenig Strahlung an die Umwelt ab. Eine Gefährdung für andere Menschen besteht dadurch normalerweise nicht. Je nach Situation empfehlen Ärzte trotzdem, für einige weitere Tage allzu engen Körperkontakt zu Schwangeren, Stillenden und Kindern zu vermeiden.
Strahlenfolgen: Mit welchen Nebenwirkungen muss man rechnen?

Im Allgemeinen gilt die Radionuklidtherapie als relativ gut verträglich und nebenwirkungsarm. Trotzdem wird auch immer gesundes Gewebe mit geschädigt, was entsprechende Symptome verursachen kann.
Was beeinflusst die Strahlenwirkung und das Nebenwirkungsrisiko?
- die Tumorart
- die genaue Lage und Ausdehnung des Tumors
- das gewählte Radiopharmakon und die Höhe der Strahlendosis
- der eigene Gesundheitszustand und das Erkrankungsstadium
Welche Strahlenwirkungen können auftreten?
Womit man tatsächlich rechnen muss und womit nicht, kann man mit den behandelnden Ärzten besprechen. Wie immer gilt: Nebenwirkungen treten vor allem dort auf, wo gesundes Gewebe mit bestrahlt wird. Ärzte unterscheiden zwischen frühen und späten Strahlenfolgen. Die frühen oder akuten Strahlenfolgen treten bereits einige Tage bis Wochen nach der Behandlung auf. Spätfolgen können sich auch erst Monate, Jahre oder sogar Jahrzehnte später bemerkbar machen.
Bei manchen Patienten führt die Behandlung mit strahlenden Medikamenten zu einer Beeinträchtigung der Blutbildung im Knochenmark. Es kann vorübergehend zu einem Mangel an roten Blutkörperchen kommen. Da dadurch der Sauerstofftransport im Körper eingeschränkt wird, ist man für einige Zeit körperlich weniger belastbar und schneller erschöpft. Seltener kommt es zu einem erhöhten Infektionsrisiko, zum Beispiel durch einen zeitweisen Verlust an weißen Blutkörperchen. Zu einer erhöhten Blutungsneigung kommt es, falls auch die Zahl der Blutplättchen sinkt.
Alle diese Veränderungen gehen nach einigen Wochen bis Monaten von alleine wieder zurück. Es kann allerdings bei einzelnen Patienten zu dauerhaften Knochenmarkschädigungen kommen. Wie bei jeder Strahlenbelastung steigt auch das Risiko für eine Blutkrebserkrankung, eine Leukämie, im Lauf des Lebens. Dieses Risiko ist an sich gering und spielt für Menschen, die erst in höherem Lebensalter behandelt werden, nur eine untergeordnete Rolle: Rein statistisch kann es Jahre und Jahrzehnte dauern, bis sich die Schädigung auswirkt. Für Kinder und Jugendliche sieht dies etwas anders aus: In den letzten Jahren sind für sie besondere Nachsorgeprogramme entwickelt worden, um möglichen Langzeitfolgen im späteren Leben rechtzeitig behandeln zu können.
Vorübergehende Schmerzen im Umfeld des Tumors sowie Allgemeinsymptome wie Übelkeit und Erbrechen können nach einer Radionuklidtherapie ebenfalls auftreten.
Während einer Schwangerschaft oder in der Stillzeit darf eine Radionuklidtherapie nicht angewendet werden, da nicht ausgeschlossen werden kann, dass das Kind im Mutterleib geschädigt würde. Das Risiko einer bleibenden Schädigung der Keimdrüsen durch die Behandlung, also der Eierstöcke bei den Frauen und der Hoden bei den Männern, ist jedoch gering. Bei Männern können durch die Therapie die Spermien beeinträchtigt werden, was selten einmal zu einer dauerhaften Zeugungsunfähigkeit führen kann. Bei Frauen können Zyklusstörungen auftreten, bei einigen setzen die Wechseljahre verfrüht ein.
Hier weitere Beispiele für mögliche Nebenwirkungen bei einer nuklearmedizinischen Behandlung:
Bei der Behandlung von Schilddrüsenkrebs: Das verbleibende Schilddrüsengewebe kann nach der Behandlung anschwellen und schmerzen. Die Bestrahlung mit radioaktivem Jod hat nur eine vergleichsweise geringe Reichweite. Trotzdem sind auch Nebenwirkungen an Mund, Rachen, Speiseröhre und Magen möglich: Die Schleimhäute können sich entzünden.
Was hilft? Gegen Schmerzen, Übelkeit und Mundtrockenheit helfen schmerzlindernde Mittel und Medikamente, die dem Unwohlsein vorbeugen. Bei Infektionen helfen Antibiotika.
Langzeitfolgen sind selten, aber nicht ausgeschlossen: Es kann zu einer Entzündung der Tränendrüsen kommen, dabei ist die Tränenflüssigkeit vermindert, die Augen sind trocken. Möglich sind auch Schädigungen der Speicheldrüsen, eine sogenannte Xerostomie oder Mundtrockenheit kann entstehen. Fehlt Speichel, wird das Essen und Schlucken schwierig, und ein trockener Mund kann auf Dauer auch zu Zahn- und Zahnfleischschäden führen. Was dagegen hilft, ist im Text Mundtrockenheit aufgeführt.
Bei der Behandlung von Knochenmetastasen: Durch die Bestrahlung kann es vorübergehend zu verstärkten Schmerzen im Knochengewebe kommen, selbst dann, wenn man an sich eine Behandlung gegen schmerzhafte Metastasen erhält. Durch die Bestrahlung verbessern sich die Schmerzsymptome jedoch meistens, und bis dahin erhält man als Patientin oder Patient Schmerzmedikamente.
Auch Beeinträchtigungen des Knochenmarks mit vorübergehenden Symptomen wie Blutarmut, Erschöpfung, Blutungsneigung oder Infektanfälligkeit sind möglich. Patienten, die gleichzeitig Bisphosphonate einnehmen, haben ein erhöhtes Risiko für eine sogenannte Kiefer-Osteonekrose. Hierbei handelt es sich um eine Schädigung des Kieferknochens. Dabei ist bislang nicht eindeutig klar, ob die Radionuklidtherapie das Risiko für diese mögliche Bisphosphonat-Nebenwirkung zusätzlich erhöht oder nicht. Patienten, die diese Medikamente erhalten, sollten sich bei den behandelnden Ärzten nach ihrem persönlichen Risiko erkundigen.
Ängste und Sorgen auffangen: Wer hilft mir, mit psychischen Belastungen umzugehen?

Viele Patientinnen und Patienten sehen der Behandlung mit strahlenden Medikamenten zunächst mit Sorge entgegen: die Angst vor der Radioaktivität oder vor Nebenwirkungen, eine eventuelle Isolation im Krankenhaus – all das kann verunsichern.
Je besser Patientinnen und Patienten über die Behandlung informiert sind, desto schneller können sich die meisten auf die neue Situation einlassen und mit den eigenen Ängsten umgehen. Experten raten daher:
- Lassen Sie sich von Ihren Ärzten über die anstehende Behandlung genau informieren: Wie läuft die Radionuklidtherapie ab? Welche Risiken gibt es?
- Sprechen Sie Ihre Ängste und Befürchtungen an!
- Suchen Sie sich psychologische Unterstützung, wenn die Angst zu groß ist!
In fast allen Kliniken gibt es die Möglichkeit, sich entsprechend beraten zu lassen. Anlaufstellen können außerdem die regionalen Krebsberatungsstellen sein. Wer längerfristig Unterstützung möchte, kann sich an einen niedergelassenen Psychoonkologen wenden.
Weitere Tipps gibt der Krebsinformationsdienst im Text Vom Umgang mit Angst: Die Zukunft zulassen.
Quellen und Links für Interessierte und Fachkreise
Sie haben Fragen zur Nuklearmedizin? Wir sind für Sie da.
So erreichen Sie uns:
- am Telefon unter 0800 – 420 30 40, täglich von 8:00 bis 20:00 Uhr, kostenlos, vertraulich
- per E-Mail an krebsinformationsdienst@dkfz.de (der Link öffnet ein gesichertes Kontaktformular)
Zum Stellenwert der Strahlentherapie bei einer bestimmten Tumorart finden Sie Angaben in den Texten unter Krebsarten.
krebsinformationsdienst.med: Service für Fachkreise aktuell – evidenzbasiert – unabhängig
Sie betreuen beruflich Menschen mit Krebs und haben Fragen? Mit dem Angebot krebsinformationsdienst.med unterstützt Sie der Krebsinformationsdienst bei Ihrer Arbeit, mit unabhängigen, aktuellen und qualitätsgesicherten Informationen. Der Service steht Ihnen von Montag bis Freitag zur Verfügung:
- telefonisch von 8:00 bis 20:00 Uhr unter 0800 – 430 40 50
- per E-Mail an kid.med@dkfz.de (der Link öffnet ein gesichertes Kontaktformular)
Genutzte Quellen
Informationen zu den für die Erstellung des Textes genutzten Quellen sowie nützliche Links sind zum Thema finden Sie im Text Hintergrund: Strahlentherapie und Nuklearmedizin – Techniken und Anwendungsbeispiele.
Weitere Themen
Erstellt: 21.03.2018
Herausgeber: Deutsches Krebsforschungszentrum (DKFZ) │ Autoren/Autorinnen: Internet-Redaktion des Krebsinformationsdienstes. Lesen Sie mehr über die Verantwortlichkeiten in der Redaktion.
Aktualität: Wir prüfen alle Inhalte regelmäßig und passen sie an, wenn sich ein Aktualisierungsbedarf durch Veröffentlichung relevanter Quellen ergibt. Lesen Sie mehr über unsere Arbeitsweise.